|
Медикаментозное лечение глаукомы
НАЦИОНАЛЬНОЕ РУКОВОДСТВО ПО ГЛАУКОМЕ
Под редакцией Е.А. Егорова Ю.С. Астахова А.Г. Щуко
Авторы и оглавление
Москва. 2008
Общие принципы
Основная задача лечения глаукомы заключается в сохранении зрительных функций и качества жизни пациента с минимальными побочными эффектами от приемлемой терапии и при приемлемой стоимости используемых препаратов.
Серьезный прогноз болезни, правильное понимание пациентами необходимости адекватного лечения и вероятность того, что назначенное лечение будет иметь продолжительный успех, являются основными задачами при формировании алгоритма терапевтического лечения больных глаукомой.
Два положения следует учесть прежде, чем осуществить выбор рациональной терапии: когда начинать лечение и как лечить. При назначении лечения следует помнить о том, что основополагающим критерием терапии является ее эффективность (потенциальное воздействие на заболевание). При этом, однако, нельзя забывать о возможности снижения эффективности лечения из-за ряда медицинских, социальных, экономических, психофизиологических и других факторов. Принципы лечения являются предметом обсуждения со стороны доктора и пациента еще и в связи с тем, что это хроническое заболевание протекает зачастую бессимптомно и требует применения одного или нескольких дорогостоящих препаратов. Мы также должны помнить, что взвешенное отношение к лечению является основополагающим фактором при назначении лекарственных препаратов: вероятные осложнения не могут преобладать перед преимуществами терапии. Врачи должны обдуманно подходить к назначению лечения, используя современные лекарственные препараты, последние достижения науки, принимая во внимание степень риска, стоимость и изменение качества жизни, учитывая особенности физического состояния и состояние зрительных функций, с целью достижения максимальной эффективности терапии в каждом конкретном случае.
Целевое давление
Тактика лечения глаукомы строится на установлении факторов риска и факта прогрессирования глаукомной оптической нейропатии и влияния на них.
Поскольку ведущим фактором патогенеза и гибели ретинальных ганглиозных клеток при глаукомной оптической нейропатии признано повышение внутриглазного давления выше индивидуально переносимого уровня основной задачей в лечении глаукомы является снижение ВГД до толерантного уровня, обозначаемое в настоящее время как целевое давление.
Целевое давление – верхний уровень тонометрического ВГД, при котором возможно остановить или замедлить повреждение внутренних структур глазного яблока и распад зрительных функций. Целевое давление не должно превышать толерантное ВГД. Целевое давление определяется с учетом всех факторов риска каждого конкретного больного в результате детального обследования и наблюдения за динамикой поля зрения и изменений диска зрительного нерва.
При выборе методов гипотензивной терапии следует учитывать следующие факторы:
- возраст больного;
- состояние ДЗН (размер и глубина экскавации, наличие прорывов к краю, цвет неврального кольца);
- состояние перипапиллярной зоны (наличие глаукоматозной перипапиллярной атрофии, перипапиллярного склероза хориоидальных сосудов, полосчатых геморрагии);
- состояние полей зрения;
- отягощенную наследственность;
- системную артериальную гипотонию или склонность к гипотоническим кризам, особенно ночным;
- склонность к возникновению спазма сосудов и мигрени;
- сердечно-сосудистые заболевания с нарушением центральной гемодинамики;
- нарушение гемодинамики в бассейне внутренней сонной артерии;
- склонность к гипергликемии;
- нарушение реологических свойств крови;
- миопию средней и высокой степени.
В соответствии с указанными факторами можно выделить группы больных с различной клинической манифестацией и тяжестью заболевания, которым будет соответствовать определенный уровень целевого давления:
- больные молодого возраста с начальной стадией ПОУГ без выраженного изменения ДЗН и перипапиллярной области, без наследственной отягощенности и сопутствующих заболеваний. Уровень «целевого давления» составляет 21-23 мм рт.ст. (при тонометрии). В ходе лечения ВГД должно быть снижено не менее чем на 20%;
- больные (независимо от возраста) с развитой или далеко зашедшей стадией глаукомы, без тяжелых сопутствующих заболеваний и наследственной отягощенности. Больные с начальными изменениями полей зрения, выраженными изменениями в ДЗН или перипапиллярной зоне, клинически значимыми сопутствующими заболеваниями и неблагоприятным семейным анамнезом. Уровень «целевого давления» составляет 17-20 мм рт.ст. (при тонометрии). В ходе лечения ВГД должно быть снижено не менее чем на 30%;
- больные с развитой и далеко зашедшей глаукомой, выраженными изменениями в ДЗН или перипапиллярной зоне, клинически значимыми сопутствующими заболеваниями и неблагоприятным семейным анамнезом. Уровень «целевого давления» составляет 16 мм рт.ст. (при тонометрии). В ходе лечения ВГД должно быть снижено не менее чем на 35-40%.
Ориентиры для выбора целевого давления у конкретного пациента
1. Для 75% здоровых лиц нормальное ВГД составляет 20-21 мм рт.ст.
2. Ориентировочные цифры для снижения тонометрического ВГД от исх02.10.2011lockquote>
I° стадия – снижение ВГД на 20% (21-23 мм рт.ст.)
I*, II°, III° стадии – снижение ВГД на 30% (17-20 мм рт.ст.)
II*, III* стадии – снижение ВГД на 35-40% (16 мм рт.ст.)
° – стадии без наследственной отягощенности и сопутствующих заболеваний,
* – стадии с клинически значимыми сопутствующими заболеваниями, неблагоприятным семейным анамнезом, выраженными изменениями в ДЗН и перипапиллярной зоне.
3. Среднее значение истинного толерантного ВГД у больных первичной глаукомой равно 16,4 мм рт.ст. и в 86% случаях не превышает 18 мм рт.ст. Зависимость толерантного ВГД (Роtl) от возраста и диастолического давления в плечевой артерии (АД диаст.):
Роtl = 14,4 – 0,025 • Возраст + 0,05 • АД диаст.
4. Для расчета предполагаемого толерантного ВГД у больных глаукомой можно использовать также формулу:
ВГД=6 + 0,1 АД ср.,
где АД сред. – среднее динамическое давление, которое рассчитываете по формуле (Wezler, Boger, 1936):
АД сред. = АД диаст. + 0,42 (АД сист. – АД диаст.).
5. Известны также кампиметрический, периметрический, окулографический, тоносфиграфический методы определения толерантного ВГД, основанные на искусственном повышении или сняжении ВГД с целью определения устойчивости зрительного нерва к изменениям офтальмотонуса по динамике зрительных функций. Индивидуально переносимым при данных тестах считается тот уровень ВГД, при котором регистрируется максимальное улучшение зрительных функций на фоне интенсивного медикаментозного снижения офтальмотонуса.
6. Предложены также способы определения толерантного ВГД и расчёта целевого давления по соотношению ВГД со средним динамическим артериальным давлением, с гемоликворным давлением и диастолическим офтальмическим перфузионным давлением, определяемых при офтальмодинамометрии, основанных на зависимости прогрессирования глаукомной оптической невропатии от кровоснабжения зрительного нерва.
Неблагоприятным для прогрессирования ГОН является увеличение градиента давления в зрительном нерве (Р зр.н.) при снижении гемоликворного давления.
Ро – Р зр.н. ? 10 мм рт.ст.
(Р зр.н. = Р цас Ч 0,61)
– Истинное внутриглазное давление (Ро) выше переносимого уровня, если его соотношение с диастолическим перфузионным давлением – Р офт.перф. / Ро меньше 1,3.
Целевое давление рассчитывается по формуле:
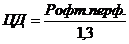
7. Если выбор целевого давления на основе вышеперечисленных факторов затруднен, считается, что ориентировочно безопасным диапазоном можно считать тонометрическое ВГД от 16 до 20 мм рт.ст.
Наиболее распространённая рекомендация заключается в первоначальном снижении ВГД на 20-30% ниже исходного уровня.
Дополнительное снижение ВГД до 40% и более определяется тяжестью поражения зрительного нерва, величиной и скоростью, с которой идёт распад зрительных функций, состоянием регионарного и системного кровообращения и другими факторами риска прогрессирования глаукомы. Более выраженные изменения требуют более низкого целевого давления.
Поскольку общепризнанного метода определения толерантного давления и целевого давления нет, ведётся его поиск в процессе наблюдения за эффективностью применяемого лечения, изменяя его в зависимости от динамики поля зрения и показателей светочувствительности в центральной зоне.
Уровень целевого давления считается достигнутым в результате лечения, если при имеющемся тонометрическом давлении не происходит дальнейшее ухудшение поля зрения и состояния диска зрительного нерва.
Уверенность в достижении целевого давления периодически проверяется сравнительным анализом состояния зрительного нерва и поля зрения с результатами предыдущих исследований.
Снижение ВГД до необходимого уровня целевого давления является ключевым моментом в эффективном лечении глаукомы.
Внутриглазное давление может быть снижено медикаментозным, лазерным и хирургическим лечением. В подавляющем большинстве случаев лечение больных глаукомой начинают с местной гипотензивной терапии.
Основные положения местной гипотензивной терапии.
1. Снижение уровня ВГД для предотвращения дальнейшего необратимого прогрессирования снижения зрительных функций;
2. Достижение целевого давления (в среднем понижение уровня ВГД на 20-30% от исходного). При этом, чем больший ущерб нанесен состоянию зрительного нерва, тем ниже должен быть уровень целевого давления. Необходим регулярный контроль соответствия тонометрического давления целевому давлению.
3. Медикаментозное лечение должно быть эффективным и достаточным для того, чтобы уверенно контролировать уровень ВГД. При этом следует помнить о т.н. эффекте тахифилаксии (т.е. привыканию к лекарственным препаратам) и необходимости своевременной коррекции проводимой терапии при выявлении малейших признаков субкомпенсации ВГД;
4. На Российском фармацевтическом рынке присутствуют практически все фармакологические группы антиглаукомных препаратов, получившие распространение в мире. В этой связи врач имеет возможность выбирать для назначения лечения патогенетически необходимые препараты, основывая при этом, в первую очередь на клинической эффективности препаратов;
5. Постоянно имея ввиду необходимость достижения эффективного лечения и имея возможность выбора препарата, следует обратить внимание на т.н. критерий «стоимость-эффективность». Этот критерий позволяет учесть и соотнести расходы и эффективность назначенной терапии. Нередко изначально более дорогие препараты являются в конечном итоге более выгодными для пациентов в том числе и из-за более эффективного и контролируемого понижения уровня ВГД;
Общие принципы выбора лекарственной гипотензивной терапии
- до лечения определяют предполагаемое целевое давление с учетом всех факторов риска, имеющихся у данного конкретного больного.
- лечение начинают с назначения лекарственного средства (ЛС) первого выбора. При его отсутствии или недостаточности эффекта данное ЛС заменяют другим ЛС или используют комбинированную терапию;
- при непереносимости или наличии противопоказаний к применению выбранного ЛС лечение начинают с использования другого ЛС;
- при проведении комбинированной терапии не следует использовать более двух ЛС одновременно; предпочтительно применение комбинированных ЛС;
- при проведении комбинированной терапии не следует использовать ЛС с одинаковым фармакологическим действием;
- адекватность достигнутого гипотензивного эффекта регулярно проверяется динамикой зрительных функций и состояния диска зрительного нерва.
- необходимо учитывать следующее: тип влияния на гидродинамику глаза, степень возможного снижения ВГД, противопоказания к применению, переносимость и необходимую частоту применения; два последних фактора могут значительно ухудшать качество жизни больных и в конечном итоге приводить к несоблюдению рекомендуемого режима лечения, что снизит эффективность проводимой терапии;
- при выборе ЛС необходимо систематическое сравнение полученного тонометрического давления с целевым давлением. ВГД не должно быть выше целевого давления;
- лечение осуществляется на протяжении всей жизни больного. При проведении медикаментозной терапии целесообразно менять ЛС. С этой целью 2-3 раза в год на 1 мес изменяют терапию. Замену следует проводить на ЛС, принадлежащее к другой фармакологической группе, с другим механизмом действия.
ЛС I выбора:
- Ксалатан 0,005% р-р - в конъюнктивальный мешок по 1 капле 1 раза в сутки, снижают ВГД до 38% от исходного уровня.
- Траватан 0,004% р-р,– в конъюнктивальный мешок по 1 капле 1 раза в сутки, снижают ВГД до 38% от исходного уровня.
- Тимолол 0,25-0,5% р-р или пролонгированного действия 0,1% гель – по 1 капле 1-2 раза в сутки. Снижает ВГД до 25-30% от исходного уровня.
ЛС II выбора:
- Бетоптик 0,5% р-р и Бетоптик-С 0,25% – по 1 капле 2 раза в сутки, снижает ВГД до 20% от исходного уровня.
- Пилокарпин 1, 2 и 4% р-р – по 1 капле до 4 раз в сутки, снижает ВГД до 17-20% от исходного уровня.
- Азопт 1% р-р – по 1 капле 2 раза в сутки, снижает ВГД до 20% от исходного уровня.
- Проксодолол 1-2% р-р – по 1 капле 2 раза в сутки, снижает ВГД до 20% от исходного уровня.
- Трусопт 2% р-р – по 1 капле 3 раза в сутки, снижает ВГД до 20% от исходного уровня.
- Клонидин 0,125, 0,25 или 0,5% р-р – по 1 капле до 3 раз в сутки, снижает ВГД до 20% от исходного уровня.
Комбинированные ЛС:
- Пилокарпин + тимолол (фотил, тимпило, фотил-форте) – по 1 капле 2 раза в сутки, снижает ВГД до 30% от исходного уровня.
- Латанопрост+тимолол (ксалаком) – по 1 капле 1 раз в день (утром), снижает ВГД до 30% от исходного уровня
- Метипранолол + пилокарпин (нормоглаукон) – по 1 капле 2 раза в сутки, снижает ВГД до 25% от исходного уровня.
Характеристика гипотензивных лекарственных средств
Современные лекарственные препараты, предназначенные для снижения ВГД при глаукоме, подразделяют по механизму действия на две основные группы: 1) лекарственные средства, улучшающие отток внутриглазной жидкости и 2) лекарственные средства, уменьшающие её продукцию.
I. Препараты, улучшающие отток внутриглазной жидкости
К ЛС, улучшающим отток водянистой влаги, относятся: простагландины F-2а, холиномиметики и симпатомиметики.
1. Простагландины F-2а
Простагландины F-2а: латанопрост (ксалатан, 0,005%), травопрост (траватан, 0,004%). Снижают внутриглазное давление за счет улучшения оттока внутриглазной жидкости по увеосклеральному пути.
Механизм гипотензивного действия: стимуляция простагландин-F-2а-рецепторов. Данные ЛС обладают самым выраженным гипотензивным эффектом среди всех других препаратов, применяемых для лечения открытоугольной глаукомы.
Латанопрост (ксалатан) является производным простагландина F-2а.. Выпускается в виде 0,005% раствора во флаконах-капельницах по 2,5 мл. Рекомендуемый режим закапывания 1 раз в сутки (вечером). Латанопрост при длительном применении по гипотензивному эффекту превосходит 0,5% раствор тимолола малеата. Длительность гипотензивного действия одного закапывания – 24 часа.
Травопрост (траватан), выпускаемый в виде 0,004%-ных глазных капель по 2,5 мл во флаконе. Травопрост – синтетический аналог простагландина FP-2?, являясь полным агонистом простагландиновых FP-рецепторов, считается одним из самых безопасных и эффективных препаратов для лечения глаукомы. По своей эффективности он не уступает, а в ряде случаев превосходит 0,005% латанопрост. Травопрост закапывают по 1 капле один раз в сутки, вечером. Длительность одного закапывания – 24 часа.
В отличие от других существующих простагландинов для лечения глаукомы, травопрост не требует специальных условий хранения. Он не теряет своих свойств от действия температуры в интервале от +2 до +25°С и света.
Местные побочные действия: гиперемия слизистой оболочки, чувство жжения, усиление роста ресниц, обратимая пигментация кожи век, при длительном лечении более 3 мес – усиление пигментации радужки (при лечении одного глаза – постоянная гетерохромия), крайне редко – отек макулы.
Побочные действия общего характера проявляются повышением АД, учащенным сердцебиением, брадикардия, боли в груди, нестабильность АД (травопрост).
Противопоказания: гиперчувствительность, беременность и кормление грудью. Не следует применять препарат у больных с вторичной поствоспалительной глаукомой, у больных, ранее перенесших воспалительные заболевания сосудистого тракта, внутриглазные операции, связанные с удалением хрусталика и повреждением задней капсулы, при макулярном отеке.
Взаимодействия с другими ЛС: выгодны сочетания с ?-адреноблокаторами, ингибиторами карбоангидразы. При совместном применении с ними усиливается гипотензивный эффект. Совместное применение с пилокарпином неоднозначен из-за возможного усиления побочных действий последнего и снижения ожидаемого гипотензивного эффекта.
2. Холиномиметики
К холиномиметикам, или парасимпатомиметикам, применяемым в офтальмологии, относятся пилокарпин гидрохлорид (1-2-4%) и карбохол (1,5% и 3%).
Пилокарпин – растительный алкалоид, получаемый из растения Pilocarpus pinnatifolius Jaborandi. Он является селективным М-холиномиметиком. Карбохол – вещество синтетического происхождения. Он с разной степенью активности действует на М- и Н-холинорецепторы.
Механизм гипотензивного действия пилокарпина: агонизм к М-холинорецепторам вегетативной нервной системы. Данные ЛС вызывают медикаментозный миоз, сокращение цилиарной мышцы, уменьшение толщины радужки, открывают доступ к дренажной зоне и улучшают отток внутриглазной жидкости. Миотики применяют при лечении как открытоугольной, так и закрытоугольной форм глаукомы, включая острый приступ.
Длительность гипотензивного эффекта при однократном закапывании раствора пилокарпина индивидуально варьирует и составляет 4-8 ч. Глазные капли пилокарпина пролонгированного действия, в которых в качестве растворителя использованы 0,5 или 1% растворы метилцеллюлозы, 2% растворы карбоксиметилцеллюлозы или 5-10% растворы поливинилового спирта, позволяют увеличить гипотензивного длительность действия до 8-12 ч при однократной инстилляции.
Из побочных действий пилокарпина следует отметить миоз, который наступает через 10-20 мин после инстилляции и длится до 6 ч, на фоне миоза может отмечаться сужение поля зрения, появление относительного спазма аккомодации через 10-30 мин после применения препарата и рост миопизации. Возможно ухудшение зрения у лиц с ядерными помутнениями в хрусталике. При длительном использовании у некоторых больных наблюдается аллергический дерматит век и конъюнктивит. У молодых пациентов с глаукомой и миопией следует избегать назначения пилокарпина из-за возможного возникновения периферических разрывов сетчатки, кровоизлияний в стекловидное тело.
Из побочных действия общего характера возможны головная боль и боль в надбровной области, бронхоспазм, боли в эпигастрии, усиление перистальтики кишечника, слюнотечение, затруднение мочеиспускания, потливость.
Пилокарпин противопоказан при гиперчувствительности к действующему веществу, иритах, иридоциклитах, иридоциклитических кризах, зрачковом блоке, ранениях роговицы, а также при сердечной недостаточности, бронхиальной астме, гипертиреозе, язвенной болезни желудка и двенадцатиперстной кишки, при сужении мочевыводящих путей с нарушением опорожнения мочевого пузыря, при беременности и кормлении грудью.
3. Адреномиметики
К данным ЛС относятся эпинефрин (адреналин гидрохлорид) 1-2%.
Механизм гипотензивного действия: агонизм к постсинаптическим ?- и ?-рецепторам вегетативной нервной системы, что проявляется улучшением оттока жидкости по дренажной системе, стимуляцией увеосклерального пути оттока, кратковременным и незначительным угнетением продукции внутриглазной жидкости.
Местные побочные явления при применении эпинефрина – мидриаз, гиперемия конъюнктивы, хронические аллергические конъюнктивиты, гиперпигментация краев век, конъюнктивы и реже роговицы, макулопатия особенно при афакии и артифакии, снижение кровоснабжения в дисках зрительных нервов.
Побочные действия общего характера проявляются повышением артериального давления, тахиаритмией, кардиалгией, цереброваскулярными расстройствами.
II. Средства, угнетающие продукцию внутриглазной жидкости
К этой группе ЛС относятся В-адреноблокаторы, центральные агонисты а2-адренорецепторов, ингибиторы карбоангидразы.
1. В1- В2-адреноблокаторы
К неселективным в-адреноблокаторам относят тимолол. Основным представителем этой группы является тимолол-малеат (0,25 и 0,5%). Известны следующие названия этого препарата: арутимол, ниолол, окумед, окупрес-Е, окурил, оптимол, офтан-тимолол, офтенсин, тимогексал, тимолол-ПОС, тимоптик, тимоптик-депо.
Механизм действия: обратимый антагонизм к в1 и в2-рецепторам вегетативной нервной системы. Данные препараты снижают образование водянистой влаги, воздействуя на непигментированные клетки цилиарного эпителия.
Снижение внутриглазного давления наступает через 20 мин после инстилляции тимолола, достигая максимума через 2-3 ч и продолжается не менее 12 ч. Рекомендуется закапывать 1-2 раза в день.
Препараты группы могут применяются при всех формах глауком.
2. Группа в1-адреноблокаторы (селективные).
Бетоксолол (бетоптик 0,5%, бетоптик С 0,25%) является избирательным препаратом. Снижая ВГД, препарат может оказывать нейропротекторный эффект.
Из побочных явлений местного характера следует отметить возникающие сразу после закапывания кратковременный дискомфорт, жжение, резь. Редко наблюдаются снижение чувствительности роговицы.
Общие побочные реакции при местном применении бетаксолола минимальны и встречаются редко. Тем не менее бетаксолол необходимо применять с осторожностью у больных, получающих перорально ?-блокаторы, резерпин; при сахарном диабете, тиреотоксикозе, бронхиальной астме.
3. Группа а- и в -адреноблокаторы
Проксодолол, 1-2% р-р – отечественный бинарный а-в-адреноблокатор выпускается в виде глазных капель с концентрацией активного вещества в растворе 1 и 2% в стеклянных флаконах по 5 мл и в тюбиках-капельницах по 1,5 мл. Снижает ВГД до 20% от исходного уровня.
Максимальное снижение ВГД до 7 мм рт.ст. наступает через 20 мин после закапывания препарата в глаз, достигает максимума через 2 ч, продолжается не менее 12 ч. Рекомендуется закапывать 1-2 раза в день.
Механизм снижения ВГД заключается в угнетении продукции внутриглазной жидкости и частично улучшении ее оттока.
Местные побочные реакции в-адреноблокаторов – сухость глаза, отек эпителия роговицы и точечный поверхностный кератит (особенное значение имеет для пользователей контактных линз). Данные побочные реакции возникают за счет уменьшения образования слезы и нарушения обменных процессов в поверхностных слоях роговицы.
Встречаются побочные реакции общего характера: брадикардия, аритмия, бронхоконстрикция, снижение артериального давления вплоть до коллапса, головокружение, мышечная слабость, депрессивные расстройства. Данные препараты противопоказаны больным с дистрофиями роговицы, сухими кератитами, бронхиальной астмой, обструктивными заболеваниями бронхов, синусовой брадикардией (<50 уд./мин), синдромом синусового узла, синоатриальной блокадой, атриовентрикулярной блокадой II-III степени, декомпенсированной сердечной недостаточностью, депрессией.
Взаимодействия
Нежелательные сочетания: с антагонистами кальциевых каналов, с ЛС, истощающими запас катехоламинов (резерпин из-за более выраженного снижения АД, брадикардия), с другими в-адреноблокаторами (усиление в-адреноблокирующего действия на сердечно-сосудистую систему), с миорелаксантами и гипогликемическими лекарственными средствами (усиление их действия).
Выгодные сочетания: с симпатомиметиками, миотиками, аналогами простагландинов F-2а, ингибиторами карбоангидразы. При одновременном использовании с ними усиливается снижение ВГД.
4. Группа ингибиторов карбоангидразы
Препараты этой группы блокируют фермент карбоангидразу, который содержится в том числе и в отростках цилиарного тела. Это приводит к уменьшению продукции внутриглазной жидкости и снижению офтальмотонуса.
Азопт – 1% раствор бринзоламида. Снижение ВГД наступает через 15-20 минут после инстилляции препарата и продолжается 12 часов. Режим инстилляций – 2 раза в день. Препарат не оказывает отрицательного влияния на дыхательную и сердечно-сосудистую системы. В случае необходимости, азопт хорошо сочетается с любыми другими препаратами для лечения глаукомы. Азопт удобен и комфортен в применении, является идеальным дополнением к простагландинам и b-бетаблокаторам в том случае, когда монотерапия этими лекарственными средствами уже не дает достаточного снижения внутриглазного давления.
Трусопт – 2% водный раствор дорзоламида гидрохлорида.
Максимальный гипотензивный эффект наступает через 2 ч после инстилляции препарата. Трусопт хорошо сочетается практически со всеми гипотензивными препаратами, потенцируя гипотензивный эффект и применяется для комплексной дополнительной терапии 2 раза в день, при монотерапии – 3 раза в день.
Местные побочные явления: чувство легкого кратковременного жжения в глазу непосредственно после инстилляции, горечь во рту, точечная кератопатия, слезотечение, светобоязнь, местные аллергические реакции.
Общие побочные действия: в редчайших случаях гемолитическая анемия, лейкопения, агранулоцитоз, уролитиаз, нарушение мочевыделения, снижения аппетита, рвота, понос, снижение веса, анорексия, парестезии, снижение либидо.
Противопоказания: аллергия на сульфаниламиды, острая почечная недостаточность, гипофункция надпочечников (болезнь Аддисона), снижение уровня кальция и калия в сыворотке крови, склонность к ацидозу, сахарный диабет.
На время лечения следует прекратить грудное вскармливание, в педиатрии следует применять с осторожностью.
Взаимодействия:
Нежелательные сочетания со следующими ЛС: с метилксантинами (эуфиллин) – потенцирование диуретического эффекта системных ингибиторов карбоангидразы; с хлоридом аммония и другими кислотообразующими диуретиками – уменьшение диуретического эффекта системных ингибиторов карбоангидразы.
Выгодные сочетания с ?-адреноблокаторами, с холинергическими препаратами. При одновременном применении с ними возможно усиление гипотензивного эффекта в отношении ВГД.
5. Центральные агонисты а2-адренорецепторов
К данным ЛС относятся клонидин, апроклонидин и бримонидин.
Механизм гипотензивного действия: агонизм к пре- и постсинаптическим а2-адренорецепторам вегетативной нервной системы. ЛС вызывает сокращение адренергических волокон цилиарной мышцы, что приводит к улучшению оттока внутриглазной жидкости, а также уменьшению секреции водянистой влаги.
Клонидин (клофелин) выпускается в виде глазных капель в концентрации 0,125, 0,25 и 0,5% в тюбиках-капельницах по 1,5 мл и флаконах по 5 и 10 мл.
Клонидин – агонист ?2-адренорецепторов (постсинаптических) головного мозга. Подавляет симпатическое влияние на эффекторные органы. При местном применении способствует уменьшению продукции внутриглазной жидкости. Гипотензивный эффект проявляется через 30 мин, максимум его наступает через 3 ч после инстилляции и сохраняется до 8 ч. Рекомендуется закапывать до 3-х раз в день. Офтальмотонус снижается в среднем на 5-9 мм рт.ст.
Лечение начинают с закапывания 0,25% раствора. При недостаточном эффекте и хорошей переносимости используют 0,5% раствор.
Гипотензивный эффект апроклонидина и бримонидина более выражен, чем у клонидина. При инстилляции 0,2% раствора бримонидина тартрата гипотензивный эффект составляет около 30%, в среднем снижение ВГД составляет 10-12 мм рт.ст., максимум действия отмечается через 2 часа, а длительность действия составляет 12 час.
Местные побочные явления клонидина: жжение в глазу, ощущение инородного тела, сухость во рту (около 20% больных), заложенность носа, гиперемия и отек конъюнктивы (15% пациентов), хронические конъюнктивиты. Аллергические реакции при применении бримонидина тартрат со стороны конъюнктивы отмечаются менее чем в 1% случаев, в меньшей степени он вызывает и общие побочные действия.
Побочные реакции общего характера – сонливость, замедление скорости психических и двигательных реакций. Реже больные отмечают нервозность, беспокойство. Могут отмечаться брадикардия, снижение АД, запоры, снижение желудочной секреции, импотенция.
Противопоказаниями для назначения ЛС этой группы являются повышенная индивидуальная чувствительность к препарату, воспалительные заболевания переднего отдела глаза и общие заболевания, такие как выраженный атеросклероз сосудов головного мозга, артериальная гипотония, выраженная синусовая брадикардия, облитерирующие заболевания периферических артерий, депрессия, антидепрессантная терапия (ингибиторы МАО, трициклические антидепрессанты).
Взаимодействия: нежелательны сочетания с антидепрессантами (снижение эффекта антидепрессантной терапии), с нейролептиками и снотворными средствами (усиление седативного и снотворного эффекта).
Выгодны сочетания с в-адреноблокаторами, совместное применение с ними усиливает местное гипотензивное действие.
Комбинированные лекарственные средства
Для повышения эффективности медикаментозного лечения глаукомы и улучшения качества жизни больных был разработан ряд комбинированных препаратов, содержащих вещества, которые обладают различным механизмом гипотензивного действия, и при одновременном применении которых наблюдается аддитивный эффект.
В офтальмологической практике наиболее часто используется сочетание в-адреноблокаторов с холиномиметиками.
Фотил является одной из наиболее широко используемых комбинаций: сочетание раствора 0,5% тимолола с раствором 2% пилокарпина (фотил, тимпило, и 0,5% тимолола с 4% пилокарпином (фотил-форте).
После инсталляции данных препаратов снижение ВГД начинается со второго часа, максимальный эффект наступает через 3-4 ч, продолжительность гипотензивного действия составляет около 12 ч. Максимальное снижение офтальмотонуса составляет 32% от исходного уровня. Рекомендуемый режим применения – 1-2 раза в день.
Местные и системные побочные реакции соответствуют реакциям, характерным для обоих препаратов в отдельности.
Ксалаком – комбинированный препарат, содержащий раствор 0,005% латанопроста и раствор 0,5% тимолола малеата. Этот препарат обладает выраженным гипотензивным действием, которое сохраняется в течение 24 ч. Его рекомендуется закапывать 1 раза в день (утром).
Нормоглаукон – сочетание 2% раствора пилокарпина с 0,1% раствором метипранолола. Метипранолол – неселективный ?-адреноблокатор, который, в отличие от тимолола, обладает слабовыраженным местным анестезирующим (мембраностабилизирующим) эффектом и кардиодепрессивной активностью.
При применении данной комбинации снижение ВГД начинается через 1 ч после однократной инстилляции, достигает максимума к 4-6 ч и сохраняется в течение 24 ч. Максимальное снижение офтальмотонуса составляет 25% от исходного уровня. Рекомендуемый режим применения – 2-3 раза в день.
Проксофелин – комбинированный препарат, включающий ?-, ?-адреноблокатор проксодолол и ?-стимулятор клонидин, оказывает потенцированное гипотензивное действие преимущественно за счет угнетения продукции ВГЖ.
При применении проксофелина снижение ВГД начинается через 0,5-1 ч после однократной инсталляции, достигает максимума через 4-6 ч и сохраняется в течение 24 ч. Максимальное снижение офтальмотонуса составляет более 10 мм рт.ст. от исходного уровня. Рекомендуемый режим применения – 2 раза в день.
Проксокарпин – отечественный комбинированный препарат, включающий 1% раствор проксодолола и 1% раствор пилокарпина.
При применении данной комбинации снижение ВГД начинается через 0,5-1 ч после однократной инстилляции, достигает максимума действия через 4-6 ч и сохраняется в течение 24 ч. Максимальное снижение офтальмотонуса составляет 5-6 мм рт.ст. от исходного уровня. Рекомендуемый режим применения – 2 раза в день.
Основные преимущества комбинированной терапии: большая гипотензивная эффективность по сравнению с монотерапией (27-33% пациентов с глаукомой или офтальмогипертензией нуждаются в дополнительном понижении уровня ВГД сразу после начала лечения, более половины пациентов, получающих ?-блокаторы (как препарат терапии первой линии) к концу второго года нуждаются в усилении гипотензивного режима); увеличение дозы препарата при монотерапии увеличивает риск возникновения побочных реакций; при сочетании различных препаратов потенцируется гипотензивный эффект; при использовании комбинированных препаратов число инстилляций уменьшается; снижается цена лечения – два препарата дороже, чем один; удобный режим применения и, следовательно, надлежащее выполнение больным назначенного лечения (выше степень соблюдения рекомендуемого режима инсталляций); качество жизни: меньше инсталляций – выше качество жизни.
Осмотические средства
Осмотические средства используются перорально и парентерально (в/в). Наиболее часто используют глицерол, маннитол, мочевину, изосорбид.
Механизм действия: осмотические (гиперосмотические) средства повышают осмотическое давление в крови, что сопровождается поступлением жидкости из тканей в кровь, в результате чего снижается внутричерепное и внутриглазное давление. Уменьшая реабсорбцию воды в проксимальных канальцах, осмотические средства обладают диуретическим эффектом.
Офтальмотонус при применении маннитола снижается через 30-60 мин, максимальное действие развивается через час и продолжается в течение 6-8 ч.
При применении глицерола снижение ВГД менее выражено, чем при использовании маннитола. Офтальмотонус снижается через 10-30 мин, максимальное действие развивается через 60-90 мин и продолжается в течение 4-5 ч.
При применении мочевины офтальмотонус снижается через 30-45 мин, максимальное действие развивается через 60 мин и продолжается в течение 5-6 ч.
При местном применении повышается осмотическое давление в слезе, что приводит к уменьшению количества экстрацеллюлярной жидкости в роговице, в результате чего исчезает ее отек.
ЛС данной группы используются для лечения следующих заболеваний: острых приступов закрытоугольной
глаукомы, вторичной глаукомы, кератопатии (местное применение при
симптоматическом лечении).
Дозы и режим введения осмотических средств определяются в зависимости от офтальмологического и общего статуса пациента.
Их используют также ля снижения ВГД при подготовке больного к операции или в послеоперационном периоде и при необходимости уменьшения отека роговицы перед обследованием (местное применение).
Переносимость и побочные эффекты: со стороны ЖКТ возможны рвота, тошнота, диарея; со стороны ЦНС – головная боль, снижение зрения, головокружение, судороги; со стороны ССС – отеки, тромбофлебит, гипотензия или гипертензия, тахикардия, боли в грудной клетке; со стороны почек осмотический нефроз, нарушение мочевыделения; метаболические нарушения – ацидоз, гипонатриемия, гиперкалиемия, дегидратация, повышение объема циркулирующей крови (ОЦК).
Противопоказания: гиперчувствительность, анурия, тяжелая дегидратация, отек легких, выраженная сердечная недостаточность, выраженные явления застоя в малом круге кровообращения, внутричерепное кровотечение.
Предостережения
Беременность, период кормления грудью
При беременности и во время кормления грудью ЛС данной группы применяют только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода и новорожденного. Следует применять с осторожностью у больных сахарным диабетом и диабетической ретинопатией, так как возможно развитие гипергликемии и глюкозурии.
Исследований безопасности применения у детей до 12 лет не проводилось.
Медикаментозное лечение в зависимости от основных типов глаукомы
Выделяют врожденные глаукомы; врожденные глаукомы, сочетающиеся с другими дефектами развития; первичные открытоугольные глаукомы; первичные закрытоугольные глаукомы; вторичные глаукомы.
Лечение острого приступа глаукомы
1. Пилокарпин, 1-6% р-р, инстилляции по 1 капле с интервалом 15 мин в течение 1-го часа, затем по 1 капле с интервалом 1ч в течение 2-3 ч, затем по 1 капле 3-6 раз в сутки.
2. Тимолол, 0,5% р-р, инстилляции по 1 капле 2 раза в сутки.
3. Возможно применение бринзоламида или дорзоламида. Бринзоламид, 1% суспензия, инстилляции по 1 капле 2 раза в сутки или Дорзоламид, 2% р-р, инстилляции по 1 капле 3 раза в сутки.
4. Ацетазоламид (диакарб) внутрь по 0,25-0,5 г 2-3 раза в сутки.
5. Глицерол, 50% р-р, внутрь 1-2 г/кг 1 раза в сутки или Маннитол, 15% р-р, в/в капельно в течение не менее 30 мин 10-13 мл/кг (1,5-2 г/кг) или 20% р-р, в/в капельно в течение не менее 30 мин 7,5-10 мл/кг (1,5-2 г/кг) или Мочевина в/в капельно медленно по 1-1,5 г/кг.
6. Фуросемид в/в или в/м 20-40 мг в сутки.
При отсутствии эффекта от терапии в течение 3-4 часов следует однократно ввести литическую смесь: хлорпромазин 2,5% р-р, в/м 1-2 мл, димедрол (дифенгидрамин) 2% р-р, в/м 1 мл или пипольфен (прометазин) р-р 50 мг в 2 мл, в/м 2 мл, тримеперидин 2% р-р, в/м 1 мл.
После введения литической смеси больному следует соблюдать постельный режим в течение 3-4 ч ввиду возможности развития ортостатического коллапса. Для купирования приступа и предупреждения развития повторных приступов обязательно проводят лазерную иридэктомию на обоих глазах. Если приступ не удалось купировать в течение 12-24 ч, то показано хирургическое лечение.
Подострый приступ
1. Пилокарпин, 1% р-р, по 1 капле 3-4 раза в течение нескольких часов, затем 2-3 раза в сутки;
2. Тимолол, 0,5% р-р, по 1 капле 2 раза в сутки;
3. Возможно применение бринзоламида или дорзоламида. Бринзоламид, 1% суспензия, по 1 капле 2 раза в сутки или Дорзоламид, 2% р-р, по 1 капле 3 раза в сутки;
В дальнейшем рекомендуется продолжить инстилляции перечисленных препаратов до выбора дальнейшей тактики лечения (лазерное, хирургическое).
4. Ацетазоламид внутрь по 0,25-0,5 г 1-2 раза в сутки, до полного купирования приступа.
Оценка эффективности лечения больных глаукомой
Критерии эффективности лечения:
- стойкая нормализация ВГД (не должно превышать толерантное ВГД);
- стабильность зрительных функций;
- отсутствие прогрессирования ГОН.
Осложнения и побочные эффекты лечения
При использовании указанных препаратов возможно развитие аллергических реакций и побочных эффектов, свойственных ЛС.
Ошибки и необоснованные назначения
Недостаточное снижение ВГД на фоне гипотензивной терапии вследствие применения неэффективных препаратов или позднего перехода к хирургическому лечению способствует прогрессированию заболевания.
Прогноз
В случае выявления заболевания на ранних стадиях и проведения адекватной гипотензивной и нейропротекторной терапии возможно сохранение зрительных функций в течение длительного времени.
Наименования групп препаратов выбора первой и второй линий монотерапии
1 линия терапии (препараты выбора)
- латанопрост, травопрост;
- тимолола малеат;
2 линия терапии (препараты выбора)
- пилокарпин.
- бетаксолол;
- проксодолол;
- бринзоламид;
- клонидин;
Алгоритм гипотензивной терапии.
Схема назначений для достижения давления «цели»
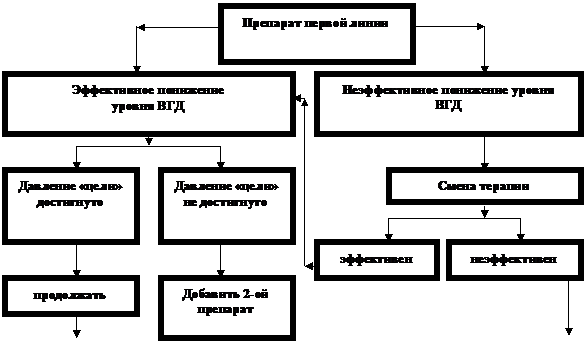
Рекомендации по мониторингу зрительных функции в зависимости от достижения давления «цели»
|
Достижение давления «цели»
|
Выявление прогрессирующих изменений
|
Временной интервал между исследованиями
|
|
Да
|
Нет
|
1-6 месяцев
|
|
Да
|
Нет
|
3-12 месяцев
|
|
Да
|
Да
|
1 неделя –
3 месяца
|
|
Нет
|
Нет
|
1 день –
3 месяца
|
|
Нет
|
Да
|
1 день – 1 месяц
|
Критерии перехода к другим методам лечения
Отсутствие компенсации уровня ВГД на оптимальном медикаментозном режиме, прогрессирующее ухудшение зрительных функций (поля зрения и состояние диска зрительного нерва), способствующих ухудшению качества жизни пациента является показанием для проведения лазерного и/или хирургического лечения. Следует помнить, что оперативное лечение может быть вариантом выбора у пациентов с впервые выявленной глаукомой в развитой или далеко зашедшей стадиях.
Режим дозирования гипотензивных препаратов,
|
Название препарата
|
Концентрация
|
Режим дозирования
|
|
Пилокарпина гидрохлорид
|
1%- 2%
|
2-4 раза в сутки
|
|
Тимолол малеат
|
0,25%- 0,5%
|
1-2 раза в сутки, однократно
утром, второе закапывание за 3 часа до сна
|
|
Бетаксолол
|
0,5%
|
1-2 раза в сутки
( время как у тимолола)
|
|
Бетаксолол С
|
0,25%
|
1-2 раза в сутки
( время как у тимолола)
|
|
Проксодолол
|
1%
|
1-3 раза в сутки
( время как у тимолола)
|
|
Клонидин
|
0,25%- 0,5%
|
2-4 раза в сутки
|
|
Проксофелин
|
|
2 раза в сутки
|
|
Фотил
|
|
1-2 раза в сутки
|
|
Дорзоламид
|
2%
|
3 раза в сутки*
|
|
Бринзоламид
|
1%
|
3 раза в сутки*
|
|
Латанопрост
|
0,005%
|
1 раз на ночь (оптимально в 20-00)
|
|
Травопрост
|
0,004%
|
1 раз на ночь (оптимально в 20-00)
|
- при комбинации с бета-блокаторами – 2 раза в сутки
Лечение детей с врожденной глаукомой.
Лечебные мероприятия, осуществляемые в отношении рассматриваемых пациентов, осуществляются в двух направлениях. Безусловно, врожденная глаукома является «хирургической патологией» органа зрения. Однако ее лечение неосуществимо без медикаментозной гипотензивной терапии, проводимой как на этапе подготовки ребенка к операции, так и, зачастую, в послеоперационный период.
Медикаментозное лечение детей с врожденной глаукомой имеет специфику, отличающую его от терапии взрослых пациентов. Главным образом, она касается недостаточного изучения фармакологического действия офтальмогипотензивных препаратов на организм детей раннего возраста. В принципе, применение большинства таких препаратов в детской офтальмологической практике возможно, когда ожидаемая польза терапии превышает потенциальный риск развития побочных эффектов.
Вместе с тем, продолжают оставаться определенные возрастные ограничения при назначении детям с врожденной глаукомой препаратов отдельных фармакологических групп. С этими оговорками мы и рассмотрим основные принципы медикаментозной терапии детей с врожденной глаукомой.
Она осуществляется в двух направлениях: стимуляции оттока внутриглазной жидкости и сокращения ее продукции. При этом возможности первого направления медикаментозной терапии при врожденной глаукоме весьма ограничены органическими изменениями угла передней камеры. Лишь использование препаратов простагландинов F2a позволило «обойти» традиционные дренажные пути, блокированные врожденными изменениями и стимулировать конкурентный увеосклеральный путь оттока водянистой влаги. Основным же направлением медикаментозной терапии при врожденной глаукоме явилось сокращение продукции внутриглазной жидкости, за счет применения ингибиторов карбоангидразы и бета-адреноблокаторов.
Традиционно медикаментозное лечение детей с врожденной глаукомой начинают с инстилляций бета-адреноблокаторов, которые при отсутствии стойкой нормализации офтальмотонуса дополняют инстилляциями препаратов простагландинов F2a, а также системным и местным назначением ингибиторов карбоангидразы. Именно в такой последовательности мы и рассмотрим основные группы офтальмогипотензивных препаратов, используемых в лечении детей с врожденной глаукомой.
Наиболее употребимыми офтальмогипотензивными препаратами при лечении детей раннего возраста служат бета-адреноблокаторы. Как правило, терапию начинают с инстилляций 0.5%- бетаксолола с частотой 2 раза в сутки. Этот препарат является селективным бета-адреноблокатором, обладающим нейропротекторными свойствами и практически не имеющим системных побочных эффектов. Вместе с тем, офтальмогипотензивный эффект 0.5%- бетаксолола (Бетоптик, Alcon) относительно невелик. Поэтому при отсутствии стабилизации офтальмотонуса в нормальных границах, 0.5%- бетаксолол заменяют одним из неселективных бета-адреноблокаторов.
Наиболее широкое распространение среди неселективных бета-адреноблокаторов в детской офтальмологической практике получили препараты тимолола малеата: Офтан-тимолол (Santen), Тимоптик (MSD), Арутимол (Bausch & Lomb), Тимолол-ПОС (Ursapharm), Окумед (Promed Exports) и др. Перечисленные выше препараты назначают детям с частотой 1-2 раза в сутки в концентрации 0.25% - 0.5%.
Вместе с тем, несмотря на относительно хорошую переносимость тимолола малеата детьми, препарат остается все же небезопасным из-за возможного развития системных побочных эффектов (бронхоспазм, апноэ, брадикардия, тревожное поведение и др.). В связи с этими обстоятельствами, детям грудного возраста, а также недоношенным детям с низкой массой тела рекомендуют ограничиваться инстилляциями 0.25%- раствора тимолола малеата. Впрочем, и в такой концентрации неселективные бета-адреноблокаторы могут вызывать серьезные системные побочные эффекты.
Мало, чем отличается от способов применения и фармакологического эффекта препаратов тимолола малеата препарат картеолола Окупресс (Cadila pharmaceuticals).
Другим направлением медикаментозной терапии детей с врожденной глаукомой служит системное и местное применение ингибиторов карбоангидразы. Наиболее широкое распространение из них получили препараты местного действия: бринзоламид (Азопт, Alcon) и дорзоламид (Трусопт, MSD). Эффект местных ингибиторов карбоангидразы на организм ребенка пока не изучен и потому их следует применять детям с осторожностью. Кроме того, их офтальмогипотензивный эффект также относительно невелик. Обычно эти препараты используют в комбинации с другими офтальмогипотензивными средствами (чаще - с бета-адреноблокаторами). Нашел также применение комбинированный препарат Косопт (тимолол-дорзоламид; MSD), более эффективный, чем его составляющие, назначенные по отдельности.
И все же наиболее широкое применение среди ингибиторов карбоангидразы при лечении врожденной глаукомы получили препараты ацетазоламида, применяемые перорально. В нашей стране эта группа препаратов представлена диакарбом (Polfarma Pharmaceutical Works SA). В педиатрической практике его целесообразно применять, ориентируясь на возраст ребенка:
- до 4 мес. – в дозе 10-15 мг/кг массы тела ребенка в сутки, разделив ее на 3-4 приема;
- от 4 мес. до 2 лет – 50 мг в сутки за 1-2 приема;
- с 2 до 4 лет – 50-125 мг в сутки за 1-2 приема;
- с 4 до 18 лет – по 125-250 мг 1 раз в сутки утром.
Диакарб в приведенной выше дозировке снижает изначально повышенный офтальмотонус на 30%-40% [Higginbotham E.J., Lee D.A., 2004]. Вместе с тем, необходимо учитывать, что этот препарат не следует применять детям в дозе, превышающей 750мг в сутки. Диакарб обладает и рядом побочных эффектов, связанных, главным образом, с потерей калия организмом: ацидозом, диареей, парестезиями, снижением аппетита и др.
Обычно диакарб назначают детям с выраженным повышением внутриглазного давления на непродолжительное время в период подготовки к операции. Если же требуется длительное применение диакарба, его обязательно комбинируют с препаратами калия. В педиатрической практике наиболее распространен калия оротат (выпускаются «детские» таблетки по 0.1г). Калия оротат назначают в дозе 10-20 мг на 1 кг веса ребенка, которую разделяют на 2-3 приема.
В последние годы в лечении детей с врожденной глаукомой все большее внимание практикующего врача привлекают препараты, относящиеся к группе простагландинов F2a. Несмотря на то, что их воздействие на организм ребенка еще окончательно не установлено, эффект таких препаратов при врожденной глаукоме очевиден и закономерно связан с усилением увеосклерального оттока водянистой влаги. Причем все эти препараты оказывают минимальный системный эффект. Вместе с тем, у детей простагландины F2a следует применять с осторожностью, руководствуясь правилом, когда ожидаемая польза от них превышает потенциальный риск развития побочных эффектов.
Побочные эффекты препаратов у детей, как правило, местные и соответствуют таковым у взрослых: усиление пигментации радужки, усиление роста ресниц, гиперемия конъюнктивы и пигментация кожи вокруг глаз. Однако наиболее серьезным побочным эффектом препаратов простагландинов F2a у детей с врожденной глаукомой служит развитие увеита (чаще – иридоциклита) и, крайне редко (у детей с афакией и артифакией), - кистозного отека макулярной области. Эти обстоятельства ограничивают применение препаратов рассматриваемой группы у детей с перенесенным увеитом или оперативным вмешательством на глазном яблоке.
Наиболее широкое распространение в лечении детей с врожденной глаукомой среди препаратов рассматриваемой группы получили латанопрост (Ксалатан, Pfiser) и травопрост (Траватан, Alcon). Оба препарата назначают однократно, по 1 капле в больной глаз вечером. По данным E.J.Higginbotham и D.A.Lee (2004), у детей с врожденной глаукомой эти препараты снижают изначально повышенное внутриглазное давление на 33% от исходного. Опыт использования ксалатана и траватана в нашей клинике свидетельствует об их достаточно высокой эффективности и безопасности в терапии детей с врожденной глаукомой [Никитина Т.Н., 2005]. Эффект препаратов повышается при их комбинации с бета-адреноблокаторами. Достаточно эффективным оказался и комбинированный препарат Ксалаком (Pfiser), содержащий латанопрост и тимолола малеат.
Прочие фармакологические группы офтальмогипотензивных препаратов в практике лечения детей с врожденной глаукомой широкого использования не получили.
Миотики (М-холиномиметики и антихолинэстеразные препараты) в лечении пациентов с врожденной глаукомой практически не используются. Это связано с тем, что сужение зрачка и оттягивание корня радужки от дренажных путей не ликвидирует причин нарушения оттока водянистой влаги при врожденной глаукоме. К тому же сопутствующий применению этих препаратов спазм аккомодации не является желательным у детей.
Симпатомиметики также не получили применения в лечении детей с врожденной глаукомой из-за неубедительной эффективности и неизученной системной токсичности для детского организма, хотя, теоретически, могли бы быть полезными в комплексной терапии таких больных [Higginbotham E.J., Lee D.A., 2004].
В целом, медикаментозная терапия детей с врожденной глаукомой служит подготовительным этапом к хирургическому вмешательству. Хотя зачастую она и используется достаточно продолжительное время (как правило, после выполненной гипотензивной операции), основным методом лечения детей с врожденной глаукомой все же является хирургический.
Заключение
Основные положения: применение современных лекарственных средств (снижение концентрации при минимальном количестве побочных эффектов и кратности применения при сохранении максимальной эффективности); применение политики информированности пациента о возможных побочных эффектах планируемой или проводимой терапии; обучение пациента навыкам правильных инстилляций, включая знания о времени и кратности закапываний, продолжительности действия назначенных препаратов, степени понижения уровня ВГД и необходимости своевременного и регулярного динамического обследования с целью непрерывного мониторинга зрительных функций; убеждение пациента в необходимости выполнения назначений и способность превратить его в союзника в лечении – это постоянные задачи, от выполнения которых будет зависеть эффективность проводимой терапии.
Оглавление:
Дата последнего обновления информации на странице 02.10.2011
|